Um sich zu vermehren, benötigen Viren eine Wirtszelle. Dort bringen sie ihre Erbinformation in Form der Nukleinsäuren DNS oder RNS ein. Diese molekularen Baupläne dienen in der Wirtszelle dafür, neue Viren herzustellen. Um fremde von eigenen Nukleinsäuren unterscheiden zu können, nutzt die Zelle eine Art Etikettier-System. Eigene RNS wird beispielsweise mit einer molekularen Kappe versehen, die sie als ungefährlich kennzeichnet. Das Immunsystem ist so in der Lage, gezielt auf Bedrohungen zu reagieren.
Die gestohlene Kappe
Bei der molekularen Kappe handelt es sich um ein methyliertes Nucleosid: Ein kleines Molekül, das an das Ende der RNS-Kette angeheftet wird. Derart markiert löst die RNA keine Immunreaktion aus. Befindet sich in der Zelle jedoch RNA, der die Kappenstruktur fehlt, wird diese vom Immunrezeptor RIG-I erkannt, und das Immunsystem wird alarmiert. Um dem zu entgehen, haben Influenza-Viren einen besonderen Mechanismus entwickelt. Sie stehlen die molekulare Kappe von zellulären RNS-Molekülen und übertragen sie auf die eigene RNS. Dieser Vorgang wird als „cap-snatching“ (Kappen-Schnappen) bezeichnet.
Influenza benötigt zelleigenes Enzym zur Replikation
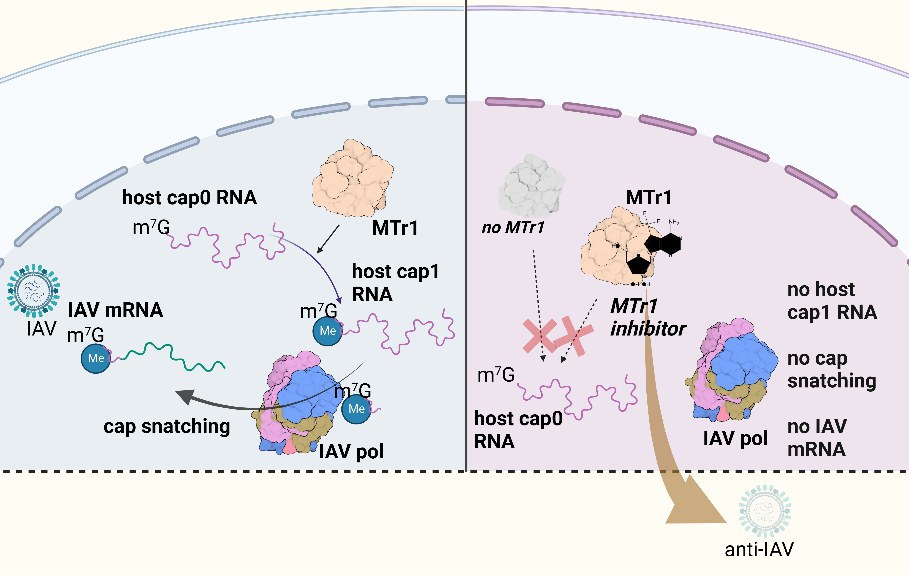
Das Enzym MTr1 versieht zelluläre mRNA mit einer Kappenstruktur und fungiert so als „Nukleinsäure-Etikettierer“ der Zelle. Das Team um Prof. Hiroki Kato vom Institut für Kardiovaskuläre Immunologie am Universitätsklinikum Bonn (UKB) konnte nun zeigen, wie sehr Influenza-Viren von der Funktion des Enzyms MTr1 abhängig sind. „Während andere Viren, wie beispielsweise auch SARS-CoV-2, in der Lage sind, ihre RNA-Moleküle selbstständig mit einer Kappe zu versehen, sind Influenza-Viren auf das Stehlen vorhandener Kappen angewiesen“, sagt Yuta Tsukamoto, Erstautor der Publikation. „Ist die Funktion von MTr1 in der Zelle gestört, stehen keine Kappen zur Verfügung, die auf virale RNS übertragen werden könnten.“ Die Aktivität von MTr1 ist somit für die Vermehrung des Influenzavirus in der Zelle essenziell.
Neuer Inhibitor hemmt Virusreplikation
Diese Abhängigkeit wollen die Forschenden für die Therapie von Influenza-Infektionen nutzbar machen. Dazu haben sie nach Inhibitoren gesucht, die MTr1 spezifisch hemmen. Das Team ermittelte, wie sich die Substanzen im infizierten Gewebe auf die Menge produzierter Viruspartikel auswirkt. Die Forschenden testeten dies sowohl im Mausmodell, als auch in menschlichem Lungengewebepräparaten. Diese so genannten Lungenexplantate stammen von Patienten, die sich einer Lungenoperation unterzogen haben. „Unter tausenden Kandidaten konnten wir ein Molekül identifizieren, das MTr1 in menschlichen Lungenexplantaten und auch in vivo in Mäusen hemmt und so die Influenza Replikation eindämmt“, berichtet Prof. Hiroki Kato, Mitglied des Exzellenzclusters ImmunoSensation2 an der Universität Bonn.
Bei dem Inhibitor handelt es sich um ein Derivat eines Naturprodukts mit der Bezeichnung Trifluormethyl-Tubercidin (TFMT), das von Bakterien der Gattung Streptomyces hergestellt wird. “Wir hoffen, dass diese Studie zur Entwicklung neuer Behandlungsmethoden für die Influenza führen wird", sagt Prof. Hiroki Kato. Dass TFMT gemeinsam mit zugelassenen Medikamenten gegen Influenza-Infektionen wirkt, konnten die Forschenden in der vorliegenden Studie bereits nachweisen. In Hinblick auf die Anzahl im Gewebe produzierter Viruspartikel konnte sogar ein klarer Synergieeffekt gezeigt werden.